全球首例基因编辑婴儿,为什么该被黑?

今早,一条爆炸性的新闻在国内生物科学界传开,南方科技大学的副教授贺建奎,突然在“第二届国际人类基因组编辑峰会”召开的前一天宣布,一对基因编辑婴儿已经于11月在中国诞生。通过特定的基因修改,她们出生之后“即能天然抵抗艾滋病”,这也是世界首例免疫艾滋病的基因编辑婴儿。
基因编辑向来会牵扯到伦理问题,贺建奎团队为此提供的伦理审核资料来自深圳一家不知名的医院——和美妇儿科医院。目前,该医院已经被证明的确属于“莆田系”医院,其创始人名为林玉明,的确是莆田系人士,并且曾在采访时明确表达自己是“莆系医院”。
消息一出,,国内生物医学界普遍持负面的态度,而普通群众则纷纷看不懂其中的过程。接下来,虎嗅就来为你解释一下为什么这次事件应该被黑。
所采用的基因编辑技术并不算突破
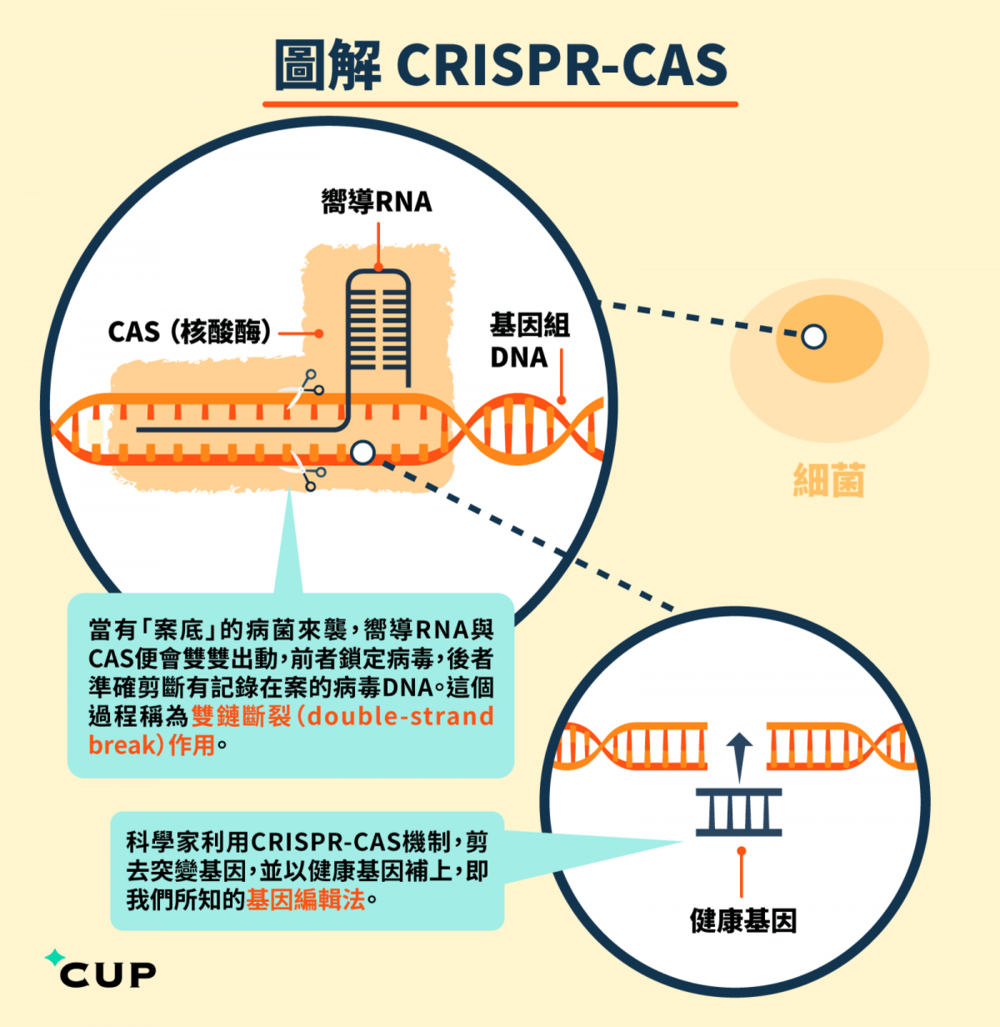
CRISPR工作原理(图自CUP)
这次婴儿基因编辑所采用的的技术名为“CRISPR/Cas9”。“CRISPR/Cas9”是目前研究最深入、应用最成熟的“基因工具”,整体原理上借助了基因的运转机制(基因最终指导蛋白质的形成),来对基因特定的片段进行编辑,其最大的突破在于编辑的环境条件很低,只需要在实验室中进行即可。
而在这次编辑中,贺建奎团队所做的主要是去除了“CCR5”基因片段上的32个碱基片段(基因的基础组成),使其便成为“CCR5 Δ32(三角形念‘Delta’)”,最终影响生成的蛋白质物质。
在基础原理之上,宏观的操作并不复杂,只比常规试管婴儿多一个步骤:在受精卵使其,将特定的物质,通过极细的针注射到单细胞的受精卵里面。
需要注意的是,本次采用的试管婴儿技术的确很成熟,但基因编辑技术至今没有尝试对人类基因进行编辑,是否能保持其他物种中的准确率仍不可知。在其上交给深圳医院的伦理审查申请书中,就专门标注了“要针对基因编辑脱靶进行监测”,但此前人类基因编辑并没有成功监测脱靶(编辑了不应该编辑的基因片段)的案例,而贺建奎团队也没有详细说明这个监测的过程和结果。
整体而言,基因编辑婴儿案例中基本使用的都是成熟的生物技术,部分全新的技术也并没有进行详细的说明解释
“CCR5 Δ32”基因防艾滋,靠谱么?
这一基因也不是本次案例的成果,而是一种普遍存在于白种人人群的基因序列,是自然界变异而生的一种基因。
根据虎嗅采访到的业内生物医学界人士解释:这种基因最近1000年左右才在白种人群众传播开来,它的出现,极有可能是欧洲数次大型瘟疫(典型的如天花)的结果,在这个过程中,拥有“CCR5 Δ32”基因的人被筛选出来。
之后人们逐渐发现白种人中拥有“CCR5 Δ32”基因的人,能够比较有效地防止“HIV-1(艾滋病病毒1型)”的传染,而“HIV-1”也是目前全球内主要传播和感染率较高的艾滋病病毒。
但目前国际上的确对于基因防控艾滋病没有太深入的研究,业内人士向虎嗅表示:“‘CCR5 Δ32’能否在白种人之外起到同样的艾滋病阻断作用没有人知道,是否会产生副作用也没人知道。”
基因编辑婴儿防艾滋,为啥要这样做?

艾滋病病毒
就目前而言,婴儿防艾滋主要是因为父母已经感染,遂采取措施防止下一代感染。除了基因编辑以外,服用阻断药物也是一个方法。根据2015年中国疾控中心的相关论文,母婴之间的艾滋病阻断花费在8.3-5万元,并且成功率高达98%以上。
相比之下,基因编辑方式中,虽然编辑基因这一环节成本很低,但是其必须在体外对受精卵进行一系列操作,同时还要保持受精卵的活性,最终还要将受精卵重新放回子宫中。整体花费上往往要超过10万,并不会更划算。
从原理上说,本次基因编辑婴儿的目的是“改变特定的蛋白质”,而阻断药物则是“用特定的蛋白质、提前和病毒对应的蛋白质结合”,原理上比较接近于“挖墙脚”。
两种方式的最终目的都是想让婴儿不被传染上艾滋病,根据澎湃新闻报道,贺建奎曾在美联社的报道中明确表示:“参与该项目的所有父亲都感染了艾滋病毒,而母亲都没有。”他同时还特别表示:“因编辑的目的不是为了防止小的传播风险,而是为感染艾滋病毒的夫妇提供一个机会,让他们有机会生下一个可能免受类似命运影响的孩子。”
有一点必须提到的是,试管婴儿还可以用于不孕不育的治疗,同时也是代孕的必须环节。目前后者在国内是违反相应法规的。
重点,严重缺失的过程
版权保护: 本文由 沃派博客-沃派网 编辑,转载请保留链接: http://www.bdice.cn/html/6464.html



